
30 Mar Tissu ressuscité
Les chercheurs de l’Institut Weizmann ont résolu un mystère vieux de 50 ans en découvrant le mécanisme moléculaire qui permet la régénération des tissus après des dommages importants. Ces découvertes pourraient ouvrir la voie à des traitements permettant de prévenir la récidive du cancer.
À l’instar d’un phénix renaissant de ses cendres, notre tissu cutané – et en fait de nombreux types de tissus épithéliaux qui tapissent et recouvrent les organes du corps – peut réagir à la mort et à la destruction par une poussée de régénération. Ce phénomène, connu sous le nom de prolifération compensatoire, a été décrit pour la première fois
dans les années 1970 chez les larves de mouches, qui ont vu repousser des ailes pleinement fonctionnelles après que leur tissu épithélial ait été gravement endommagé par une forte dose de rayonnement. Depuis lors, cette capacité surprenante a été documentée chez de nombreuses espèces, y compris chez l’homme, mais son fondement moléculaire reste flou.

(l-r) Dr. Tslil Braun and Prof. Eli Arama
Une nouvelle étude de l’Institut Weizmann des sciences, publiée dans Nature Communications, révèle que les enzymes responsables de la destruction cellulaire, les caspases, peuvent également rendre certaines cellules résistantes à la mort, permettant ainsi aux tissus endommagés non seulement de se régénérer, mais aussi de devenir plus résistants.
Malheureusement, ce même mécanisme peut être détourné par de nombreux types de cancer et pourrait expliquer pourquoi certaines tumeurs réapparaissent sous une forme plus agressive et résistante aux traitements. Ces nouvelles découvertes pourraient donc ouvrir la voie à des thérapies qui accélèrent la cicatrisation des plaies et aident à prévenir les récidives du cancer.
La forme la plus courante de mort cellulaire dans un organisme sain est l’apoptose, un « suicide » programmé déclenché lorsqu’une cellule vieillit, est endommagée ou reçoit des signaux lui ordonnant de mettre fin à sa vie. Au cours de ce processus, une caspase initiatrice déclenche la voie de la mort en activant des caspases effectrices, qui découpent alors les protéines de la cellule en petits morceaux. Au cours des deux dernières décennies, des études menées dans le monde entier, notamment dans le laboratoire du professeur Eli Arama du Département de Génétique Moléculaire de l’Institut Weizmann, ont établi que les caspases apoptotiques jouent un rôle crucial non seulement dans la mort cellulaire, mais aussi dans des processus essentiels à la vie. Ces découvertes ont conduit Arama, l’un des pionniers de la recherche sur les rôles non létaux des caspases, à émettre l’hypothèse que les caspases pourraient également être responsables du phénomène mystérieux de la prolifération compensatoire.
Dans cette nouvelle étude, une équipe dirigée par le Dr Tslil Braun, du laboratoire du Prof. Arama, a reproduit l’expérience initiale qui avait permis de découvrir ce phénomène, à savoir l’irradiation de larves de mouches à fruits par des rayonnements ionisants. Cette fois-ci, cependant, des technologies génétiques avancées ont permis aux chercheurs de suivre la régénération épithéliale avec un niveau de détail sans précédent. « Nous avons cherché à identifier les cellules qui appuient sur le bouton d’autodestruction mais survivent malgré tout », explique le Dr Braun. « Pour ce faire, nous avons utilisé un capteur retardé qui signalait les cellules dans lesquelles la caspase initiatrice avait été activée, mais qui avaient néanmoins survécu à l’irradiation. C’est ainsi que nous avons découvert une population de cellules que nous avons baptisées « cellules DARE ». Non seulement ces cellules ont survécu à l’irradiation, mais elles se sont multipliées, ont réparé les tissus endommagés et en ont reconstitué près de la moitié en 48 heures. » Mais qu’en est-il du reste des tissus en régénération ?
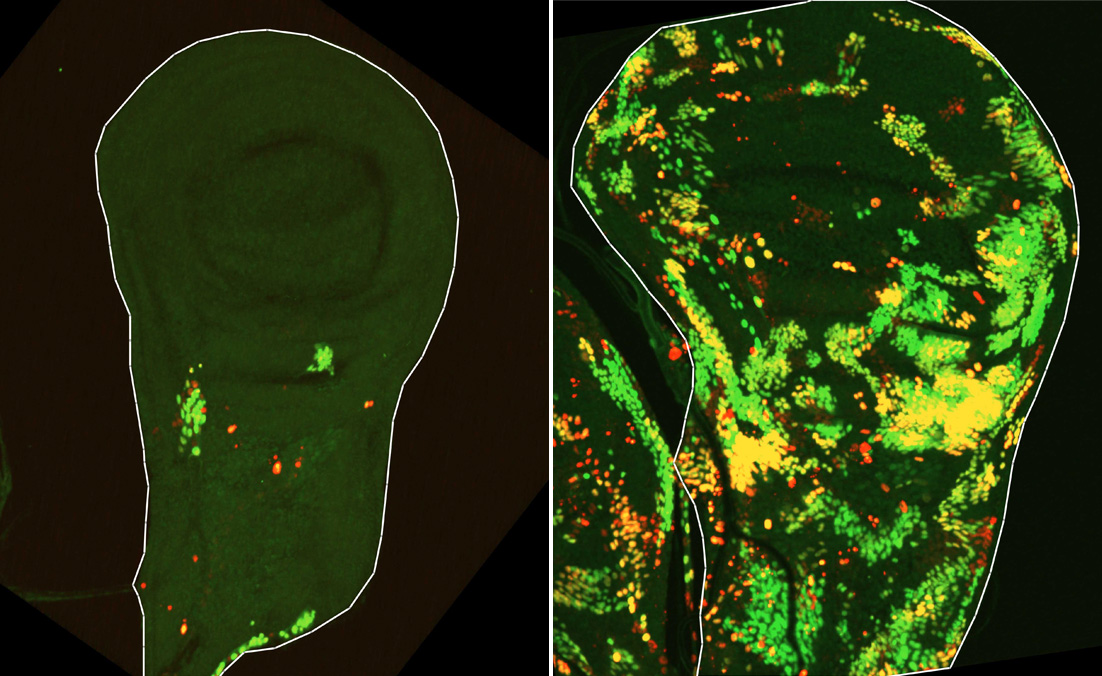
Tissu épithélial à partir duquel se développe l’aile de la mouche. Quatre heures après l’irradiation de ce tissu, on peut observer un petit nombre de cellules DARE résistantes à la mort qui ont survécu (à gauche, marquées en rouge). Après environ 24 heures, le nombre de ces cellules atteint son maximum, et après 48 heures, leurs descendantes (à droite, marquées en vert et jaune) repeuplent le tissu.
« Nous avons identifié une autre population de cellules résistantes à la mort, mais contrairement aux cellules DARE, elles ne présentaient aucune activation de la caspase initiatrice. Nous les avons appelées cellules NARE », explique Braun. « Bien que les cellules NARE contribuent finalement à la régénération tissulaire, elles ne peuvent pas le faire seules : lorsque nous avons retiré les cellules DARE du système, la prolifération compensatoire a complètement disparu. Nous avons également découvert que les cellules mourantes dans le tissu jouent un rôle dans l’explosion de régénération : les cellules DARE ont été activées par des signaux provenant de leurs voisines mourantes. »
Les chercheurs ont ensuite cherché à comprendre comment les cellules DARE survivent à des doses de rayonnement qui déclenchent l’apoptose dans les cellules voisines. « Nous avons observé que, bien que la caspase initiatrice soit activée dans ces cellules, le processus de mort cellulaire s’arrête là et ne passe pas à l’étape suivante », explique Arama. « Nous avons soupçonné qu’une protéine connue sous le nom de moteur moléculaire en était responsable : elle peut fixer la caspase initiatrice à la membrane cellulaire, l’empêchant ainsi d’activer les caspases exécutrices. En effet, lorsque nous avons désactivé cette protéine motrice, les cellules DARE ont commencé à mourir et la régénération tissulaire a été altérée.
On sait que les tumeurs qui repoussent après une radiothérapie deviennent souvent plus agressives et plus résistantes au traitement. « Nous voulions comprendre si la résistance à la mort est héritée par les descendants des cellules résistantes à la mort qui ont survécu à l’irradiation initiale », explique le Prof. Arama. « Nous avons découvert que lorsque le même tissu est irradié une deuxième fois, le nombre de cellules qui meurent au cours des premières heures est deux fois moins élevé qu’après la première irradiation, et la plupart des cellules mortes appartiennent à la population NARE. En d’autres termes, les descendants des cellules DARE se sont révélés exceptionnellement résistants, sept fois plus résistants à la mort cellulaire que les cellules du tissu d’origine. Cela pourrait expliquer pourquoi les tumeurs récurrentes deviennent plus résistantes après une radiothérapie. »
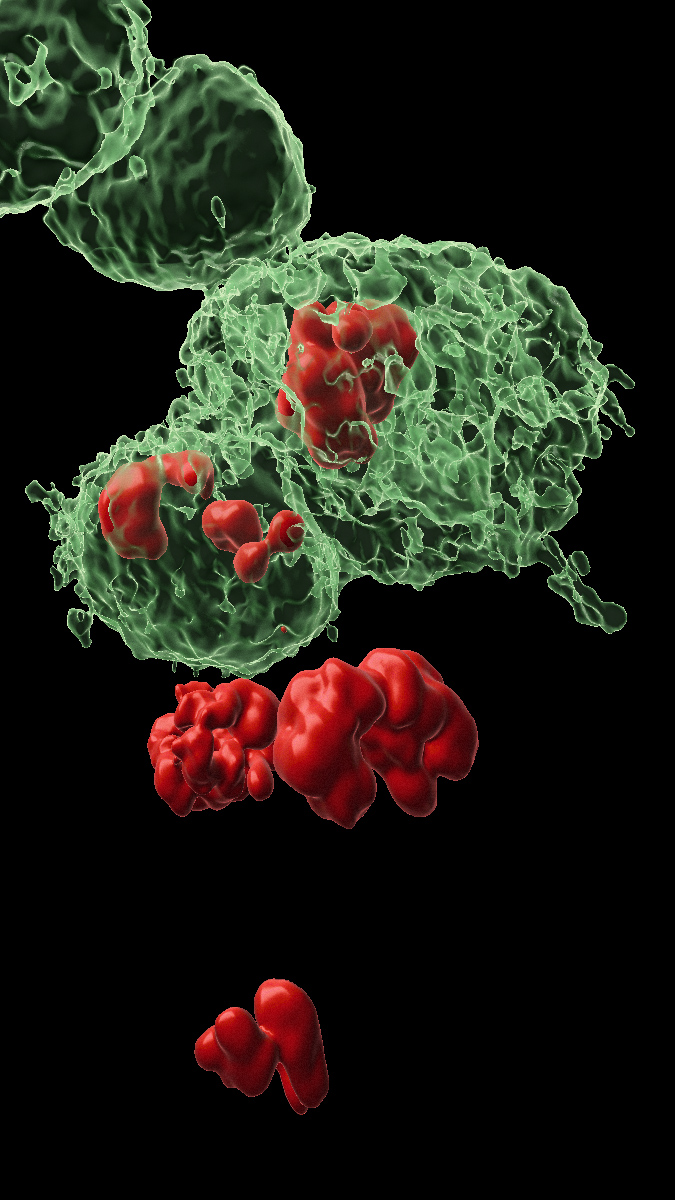
Cellules DARE (marquées en vert) et cellules NARE (non marquées) dans le tissu épithélial à partir duquel se développe l’aile de la mouche. En rouge, les noyaux des cellules en cours de division. Les chercheurs ont découvert que les cellules NARE reçoivent des signaux des cellules DARE voisines leur ordonnant de proliférer.
Un équilibre délicat entre la réparation tissulaire et la croissance excessive est essentiel à tout processus régénératif. Dans la dernière partie de leur étude, les chercheurs ont révélé comment la croissance incontrôlée est empêchée pendant la réparation tissulaire après une lésion. « Les cellules DARE favorisent la croissance des cellules NARE voisines, apparemment en sécrétant des signaux de croissance », note Arama. « À leur tour, les cellules NARE sécrètent des signaux qui inhibent la croissance des cellules DARE. En fait, nous avons découvert une boucle de rétroaction négative entre les deux populations cellulaires qui empêche la croissance excessive. »
« Nous espérons que, comme cela a souvent été le cas avec les modèles de mouches, les connaissances acquises ici pourront être traduites en une compréhension des mécanismes qui équilibrent la croissance et confèrent une résistance à la mort cellulaire dans les tissus humains », conclut le Prof. Arama. « De nombreux cancers trouvent leur origine dans des cellules épithéliales qui ont perdu leur contrôle normal de croissance, et de nombreux traitements traditionnels contre le cancer visent à les autodétruire par apoptose. Nos découvertes ouvrent la voie à la compréhension des raisons pour lesquelles ces traitements échouent parfois et de la manière dont ils pourraient être améliorés. Les résultats indiquent également de nouvelles façons dont nous pourrions accélérer la régénération bénéfique des tissus sains après une lésion. »
La Science en Chiffres
Bien que le traitement par rayonnement ionisant ait été introduit dès la fin du XIXe siècle, il reste l’un des principaux traitements contre le cancer, utilisé chez 50 à 60 % des patients à un certain stade de leur maladie.


