14 Sep Les différents types d’« associés » du cancer
Les acteurs qui aident la croissance d’un cancer pourraient aussi aider à prédire le parcours de la maladie.
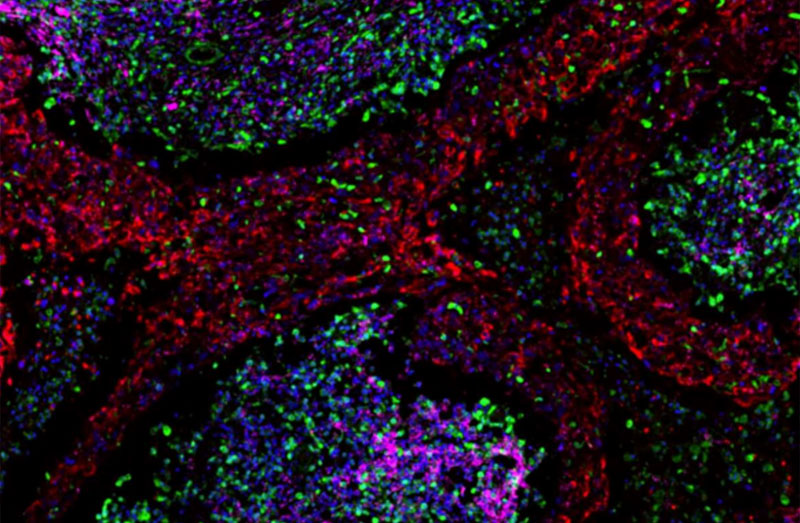
Échantillon de tissu d’un cancer du sein triple négatif, coloré pour distinguer les cellules cancéreuses (rouge) et les deux types de fibroblastes associés au cancer : pCAFs (magenta) et sCAFs (vert). Les noyaux de toutes les cellules sont en bleu.
Les seconds rôles portent parfois la pièce – au théâtre comme dans le cas du cancer. En effet, c’est « grâce à » des cellules de soutien appelées fibroblastes, associées au cancer, que le cancer du sein se développe. Il serait même possible de prédire l’évolution de la maladie à partir des types de fibroblastes présents au sein d’une tumeur. Cette conclusion ressort d’une étude menée par des chercheurs de l’Institut Weizmann des Sciences.
Les fibroblastes associés au cancer (CAFs) sont présents en grande quantité dans les cancers du sein et d’autres tumeurs solides cancéreuses. Par exemple, dans le cas du cancer du pancréas, ils représentent plus de 90 pour cent du tissu tumoral. Contrairement aux cellules cancéreuses, les fibroblastes dans les tumeurs ne subissent pas de mutations mais l’expression de leurs gènes est différente de celle des cellules saines, tout comme le rôle qu’ils jouent. Ils libèrent des protéines qui modifient la réponse immunitaire, stimulent la croissance des vaisseaux sanguins et construisent la matrice extracellulaire qui maintient les cellules ensemble. Le docteur Ruth Scherz-Shouval du département des sciences biomoléculaires de l’Institut Weizmann a entrepris de découvrir comment l’expression génétique dans les fibroblastes se modifie dans le cas de la malignité, jusqu’à quel point ces changements sont variés et dynamiques et comment ils affectent le fonctionnement des cellules.
Les changements dans l’expression génétique d’une cellule se reflètent dans la nature et la quantité de ses ARNs. Dans le laboratoire du docteur Scherz-Shouval, Gil Friedman a cherché à caractériser les fibroblastes de tumeurs du sein chez des souris. En collaboration avec d’autres membres de l’équipe et avec le laboratoire du professeur Ido Amit, du département d’immunologie, les scientifiques ont séquencé l’ARN de centaines de cellules provenant de tumeurs à différents stades de croissance, dont la métastase, et ont analysé les données de séquençage afin de comprendre comment les fibroblastes se relient dynamiquement à la tumeur.
Les chercheurs ont découvert que les fibroblastes associés au cancer pouvaient être classés en différents sous-types, chacun caractérisé par un modèle d’expression génétique particulier produidant un ensemble différent d’ARNs. Globalement, ils peuvent être regroupés en deux types majeurs appelés « p » et « s ». Les fibroblastes de la catégorie « p », appelés pCAFs, se développent dans le tissu sain autour de la tumeur, ceux de la catégorie « s », sCAFs, se développent ailleurs, probablement dans la moëlle osseuse.
En isolant ces deux types de fibroblastes à partir de tumeurs prélevées chez des souris et en les étudiant dans des cultures tissulaires, les scientifiques ont découvert une répartition des tâches entre catégories : les différences d’expression génétique se retrouvent dans les différents rôles joués par les CAFs dans la malignité. De plus, l’expression génétique comme le rôle de ces cellules sont dynamiques – ils changent avec la progression de la tumeur. Par exemple, dans les stades précoces de la croissance tumorale, un sous-type des pCAFs supprime principalement l’activation des lymphocytes T, mais dans les stades plus tardifs, la fonction principale de ces pCAFs est de libérer du collagène pour former la matrice extracellulaire.
Afin de tester la pertinence de ces découvertes dans le cas des êtres humains, les scientifiques ont analysé des échantillons de tissus issus de centaines de patientes atteintes d’un cancer du sein collectés au Centre médical Chaim Sheba à Tel Hashomer, Israël, et au Cancer Research UK à Cambridge. Les chercheurs ont suivi une procédure particulièrement adaptée aux conditions hospitalières : colorer les tissus des échantillons avec différents marqueurs en fonction des sous-types cellulaires, en se basant sur ceux qu’ils avaient identifiés dans les cellules de souris. La coloration a révélé des similitudes entre les fibroblastes des tumeurs des souris et ceux des humains, les deux sous-types pCAFs et sCAFs étant présents. De plus, le ratio entre ces deux types de cellules était corrélé avec le pronostic de la maladie : le taux de survie était nettement plus élevé chez les patientes présentant plus de sCAFs que de pCAFs. Cette dernière découverte était flagrante chez les patientes atteintes d’un cancer du sein triple négatif et présentant des mutations du BRCA, soit l’un des types de cancer du sein les plus agressifs, particulièrement présent dans la communauté juive ashkénaze.
 (de gauche à droite) Coral Halperin, Shimrit Mayer, Yanis Stein, Gil Friedman, Hagar Lavon, docteur Ruth Scherz-Shouval, Oshrat Levi-Galibov et docteur Meirav Pevsner-Fischer
(de gauche à droite) Coral Halperin, Shimrit Mayer, Yanis Stein, Gil Friedman, Hagar Lavon, docteur Ruth Scherz-Shouval, Oshrat Levi-Galibov et docteur Meirav Pevsner-Fischer
En plus d’apporter un moyen d’établir le pronostic d’un cancer du sein, les découvertes de cette étude ouvrent de nouvelles voies pour la recherche de potentielles futures thérapies ou pour améliorer des thérapies existantes. Des recherches plus approfondies permettront de mieux comprendre comment exactement les fibroblastes affectent le microenvironnement de la tumeur ce qui pourra aider à développer de nouveaux médicaments. Par exemple, la modification de la réponse immunitaire par les fibroblastes pourrait être bloquée par des traitements ciblés permettant aux cellules immunitaires, notamment celles induites par les différentes immunothérapies, de tuer les tumeurs.
Différents chercheurs ont participé à cette étude : Oshrat Levi-Galibov, Coral Halperin, le docteur Meirav Pevsner-Fischer, Hagar Lavon, Shimrit Mayer, le docteur Reinat Nevo et Yaniv Stein du département des sciences biomoléculaires ; Eyal David et les docteurs Chamutal Bornstein et Amir Giladi du département d’immunologie ; le docteur Avi Mayo et le professeur Uri Alon du département de biologie cellulaire et moléculaire ; les docteurs Maya Dadiani, Nora Balint-Lahat, Iris Barshack et Einav Nili-Gal-Yam du Centre médical Chaim Sheba ; et les docteurs H. Raza Ali et Carlos Caldas du Cancer Research UK
Les recherches du docteur Ruth Scherz-Shouval sont financées par le Centre intégré Moross pour le cancer, le fonds de la famille Laura Gurwin Flug, la bourse Peter et Patricia Gruber, la fondation Rising Tide, la fondation de la famille Elsie et Marvin Dekelboum et la succession Aliza Yemini. Le docteur Scherz-Shouval est détentrice de la chaire Ernst et Kaethe Ascher pour le développement de carrière en sciences de la vie.


